Tým 23 brněnských vědců se významně přiblížil odpovědi na otázku, jak předcházet a jak léčit Alzheimerovu nemoc, která bývá nejčastější příčinou demence a vede postupně k závislosti nemocného na každodenní pomoci jiného člověka. Odborníci z Přírodovědecké a Lékařské fakulty MUNI, ICRC a Masarykova onkologického ústavu věří, že výsledky výzkumu pomohou vyvinout další vysoce účinné léčivé látky pro tuto civilizační hrozbu 21. století.
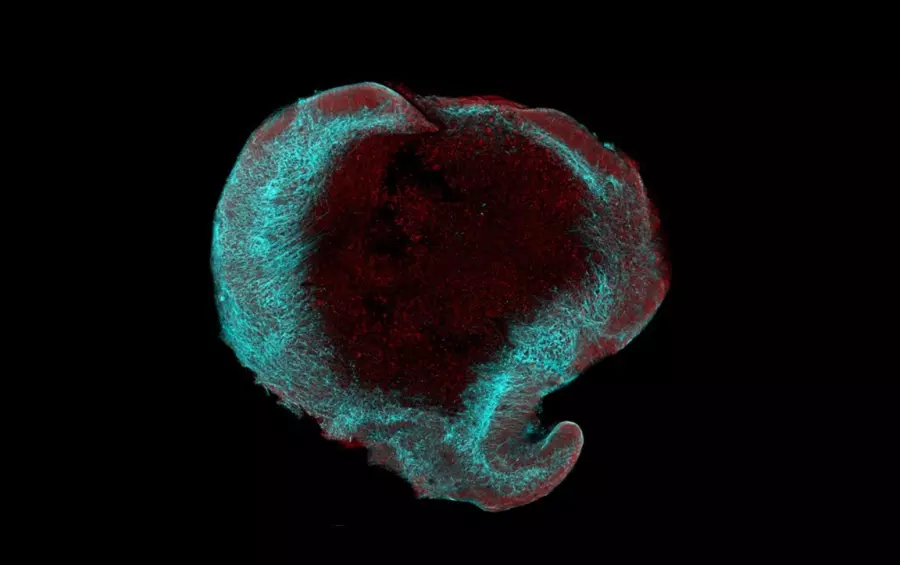
Mikroskopický snímek mozkového organoidu. Experimenty s laboratorně kultivovanými mozkovými organoidy prokázaly pozitivní efekt homotaurinu a dávají naději, že jsme blíže k léčbě Alzheimerovy demence. Ve světě se již vědci zabývají tím, jak využít vlastnosti homotaurinu v prevenci či léčbě kognitivních onemocnění a objev brněnských vědců nyní posouvá tyto snahy blíže ke klinické praxi.
„Klíčovou roli v rozvoji Alzheimerovy demence má apolipoprotein E (ApoE), který se vyskytuje také v mozkové tkáni. Objevili jsme molekulární podstatu nežádoucího hromadění tohoto apolipoproteinu a současně jsme ukázali způsob, jak je možné toto hromadění ApoE potlačit potenciálním léčivem, které je již v pokročilé fázi klinického testování s předpokládaným schválením v roce 2025,“ shrnul hlavní význam výzkumu molekulární biolog Martin Marek, který působí v Loschmidtových laboratořích centra RECETOX Přírodovědecké fakulty Masarykovy univerzity a v Mezinárodním centru klinického výzkumu (ICRC), které je společným pracovištěm FN u sv. Anny v Brně a Lékařské fakulty Masarykovy univerzity.
Právě ApoE hraje důležitou roli ve fungování mozku a je též znám jeho protizánětlivý vliv. V lidské populaci jsou však rozšířeny tři varianty: ApoE2, ApoE3 a ApoE4. Již dříve bylo prokázáno, že hlavním rizikovým faktorem pro vznik Alzheimerovy choroby je přítomnost varianty ApoE4. Zdědění varianty ApoE4 totiž významně zvyšuje riziko Alzheimerovy demence. U pacientů se dvěma kopiemi genu pro ApoE4 dochází k většímu poškození paměti, snížení schopnosti běžné každodenní činnosti a k výraznější atrofii mozkové tkáně. O objasnění tajemství ApoE4 se vědci z celého světa pokoušejí již několik desetiletí, avšak až brněnští vědci nyní nahlédli pod pokličku této molekulární záhady.
„Vzrušující na tomto výzkumu bylo, že toxická varianta ApoE4 se liší od svých netoxických protějšků jen jednou mutací, která má ovšem obrovské důsledky v chování proteinu a vztahu k rozvoji Alzheimerovy demence,“ vysvětlil Marek.
Významnou součástí studie byl také výzkum, jak nežádoucímu ukládání ApoE4 v mozkové tkáni předcházet, a tak obnovit jeho důležité buněčné funkce. Laicky řečeno – jak zabránit nebo zpomalit rozvoj nemoci a zachovat myšlení a paměť. V navazujících biochemických experimentech výzkumníci prokázali, že existuje látka homotaurin, derivát aminokyselin, nacházející se v některých druzích mořských řas, která potlačuje nežádoucí hromadění a obnovuje původní funkce v ApoE4 proteinu, a mohla by tak mít „léčebný“ efekt i v klinické praxi.
Při experimentech vědci používali mozkové organoidy, což jsou „minimozečky“ vypěstované ve zkumavce z buněk pacientů s Alzheimerovou chorobou. „Mozkové organoidy jsme v této studii použili pro testování účinku homotaurinu na rozvoj Alzheimerovy demence. Naše výsledky potvrzují, že léčivo má pozitivní efekt na organoidy s variantou ApoE4, a ukazuje se, že ovlivňuje nejen důležité signalizační dráhy, ale také metabolismus cholesterolu. V dalších studiích se chceme zaměřit na podrobné mapování změn, které homotaurin v lidském mozku způsobuje,“ nastínila budoucí terapeutický efekt homotaurinu a další směr výzkumu buněčná bioložka Dáša Bohačiaková z Ústavu histologie a embryologie Lékařské fakulty MU.
Brněnským vědcům se podařilo kombinací experimentálních a výpočetních experimentů detailně zmapovat strukturní změny v ApoE proteinu na atomární úrovni. Díky těmto změnám není varianta proteinu ApoE4 stabilní, má vysokou tendenci k nežádoucímu hromadění v mozkové tkáni a ztrácí tak svou primární úlohu v přenosu lipidů a cholesterolu.
„Dynamické změny ve strukturách ApoE3 a ApoE4 proteinů a jejich interakce s potenciálním léčivem (homotaurinem) jsme sledovali pomocí unikátní metody výměny vodíku za deuterium spojené s hmotnostní spektrometrií. Výsledky odhalily přestavbu struktury u ApoE4 způsobující agregaci, která však nebyla pozorována u ApoE3. Naopak interakce s léčivem strukturu ApoE4 stabilizovala, a tím potlačila její negativní vlastnosti,“ doplnila biochemička Lenka Hernychová z centra RECAMO Masarykova onkologického ústavu.
Brněnští vědci publikovali výsledky svého výzkumu v prestižním odborném časopise Molecular Neurodegeneration. Výzkum získal podporu MŠMT v rámci projektů ENOCH a INBIO. Finančně výzkum podpořila i Evropská unie v rámci programu Horizon Europe granty TEAMING a ADDIT-CE.
„Studie byla unikátní, protože se klasické metody molekulární a buněčné biologie podařilo doplnit o data získaná technikou hmotnostní spektrometrie. Takto lze velmi citlivě a přesně sledovat změny v hladinách proteinů a lipidů a nahlédnout do mechanismu účinku potenciálních léčiv. Zároveň lze pomocí hmotnostní spektrometrie charakterizovat často heterogenní buněčné modelové systémy,“ popsal jedinečnost tohoto výzkumu analytický chemik Zdeněk Spáčil z centra RECETOX Přírodovědecké fakulty Masarykovy univerzity.
Zdroj: Masarykova univerzita
- Autor článku: ne
- Zdroj: Masarykova univerzita











































