V červnu 2022 nabídla Evropská výzkumná rada (ERC) financování dalšímu českému projektu. V prestižním programu ERC Consolidator Grants uspěla Alena Zíková z Biologického centra AV ČR. Zabývat se bude základními buněčnými mechanismy, které umožňují komunikaci uvnitř buňky.

Molekulární bioložka Alena Zíková z Parazitologického ústavu Biologického centra AV ČR získala prestižní evropský grant v programu ERC Consolidator Grants. Evropská rada pro výzkum (ERC) na začátku června navrhla její vědecký projekt k pětiletému financování ve výši dvou milionů eur. Alena Zíková bude studovat mechanismy, které umožňují komunikaci uvnitř buňky.
Vzhledem k tomu, že se jedná o základní buněčný proces, budou mít nové poznatky přesah do mnoha odvětví biologie, včetně lidské medicíny. Můžou například pomoci rozkrýt podstatu zhoubných procesů jako je stárnutí, neurodegenerativní nemoci či rakovina.
Komunikace uvnitř buňky
Hlavním témata projektu Aleny Zíkové je množství komunikační mechanismů uvnitř buňky. Jádro buňky například naslouchá buněčným organelám a na základě poskytnutých informací se rozhoduje, co dál podniknout. Možností je spousta, buňka se může rozdělit, nebo se změnit v jiný typ buňky, může „usnout“ a čekat na lepší vnější podmínky, či spáchat buněčnou sebevraždu.
Jednou z nejdůležitějších organel, které mají na buněčný osud vliv, jsou mitochondrie. Tyto buněčné továrny poskytují buňce nejenom energii, ale také vyrábí řadu důležitých látek. Zbytku buňky neustále podávají zprávy o tom, jak se jim daří, co vyrábí a zda můžou dodat dostatek energie pro daná buněčná rozhodnutí.
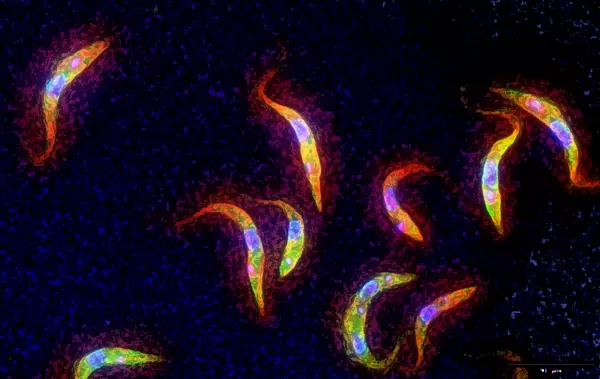
Na snímku obarvené buňky Trypanosoma brucei: DNA (jádro a kinetoplast) – modře, cytosol – zeleně, mitochondrie – oranžově, foto: Minal Jain, Biologické centrum AV ČR
Kyslíkové radikály – kdy jsou životně nezbytné a kdy škodí?
Informace se předávají pomocí nejrůznějších molekul. Jedněmi z nich, jak se teprve nedávno překvapivě zjistilo, jsou i reaktivní molekuly kyslíku (reactive oxygen species, ROS), nazývané také jako kyslíkové radikály. Ve vědě jsou tyto molekuly dobře známy, protože pokud je jich v buňce nadbytek, způsobují rozsáhlá poškození, tzv. buněčný stres, který může končit až smrtí buněk. Proto se také nadměrná produkce ROS molekul nejčastěji studuje ve spojení s řadou zhoubných procesů, jako je např. stárnutí, neurodegenerativní nemoci, či rakovina.
Málo je však probádaná životně důležitá role kyslíkových radikálů v buněčné komunikaci. Navíc molekulární procesy, které ji doprovázejí, jsou dosud neznámé, ač se jedná o jeden z nejzákladnějších buněčných dějů.
Alena Zíková se ke studiu kyslíkových radikálů dostala vlastně náhodou při výzkumu jednobuněčného parazita Trypanosoma brucei, který způsobuje spavou nemoc. „Studovali jsme, jak se parazit mění z jednoho vývojového stádia do dalšího v mouše Tse-Tse, a protože se zaměřujeme na mitochondrii, všimli jsme si, že tato změna je spojená s vyšší produkcí radikálů kyslíku. To pro nás bylo velice zajímavé zjištění. Obvykle totiž tyto molekuly buňce škodí, ale v tomto případě jí pomáhaly, aby se z ní stal nový typ buňky,“ říká bioložka s tím, že bude řešit, jak radikály kyslíku tuto přirozenou buněčnou změnu provádějí.
Parazit se pro laboratořní účely chová v živném médiu, foto: Daniela Procházková, Biologické centrum AV ČR
Parazit jako pokusný králík
Použít k výzkumu vnitrobuněčné komunikace trypanozomu se ukazuje jako unikátní a elegantní řešení, které nabízí oproti klasickým modelovým organismům hned několik výhod. Zaprvé je parazit tvořen jedinou buňkou, která se při vývoji přirozeně přeměňuje do různých buněčných typů. Zadruhé má pouze jednu velkou mitochondrii (oproti např. buňkám savců, které jich obsahují desítky) a tato organela se během vývojových fází výrazně mění.
Tým Aleny Zíkové využije při výzkumu nejmodernější biologické metody a nástroje, k nimž patří hmotnostní spektrometrie nebo metodologie tzv. genetických nůžek (CRISPR/Cas9). Geneticky modifikovaní paraziti ve spojení s různými látkami umožní cíleně měnit množství kyslíkových radikálů v mitochondrii i v cytoplasmě tak, aby vědci mohli sledovat, jaké změny to u parazita způsobí.
Nové poznatky pomůžou i v medicíně
Díky ERC grantu mají českobudějovičtí vědci jedinečnou příležitost využít svých bohatých zkušeností s modelovým organismem Trypanosoma brucei, a přispět tak k objasnění základních molekulárních mechanismů buňky. „Tím, že se jedná o natolik základní a evolučně starý proces, bude stejný pro ostatní organismy, včetně člověka. Jsme přesvědčení, že naše poznatky budou mít velký přesah a umožní objasnit hranici mezi tím, kdy jsou kyslíkové radikály životně důležité pro správnou funkci buňky a kdy už naopak škodí,“ vysvětluje Alena Zíková.
Tyto informace v budoucnu pomůžou rozkrýt podstatu nemocí, které způsobuje stres a nadprodukce reaktivních molekul kyslíku, a budou velice důležité při studiu účinků různých antioxidantů a jejich využití v léčbě řady lidských onemocnění.
O podporu svého výzkumného projektu v programu ERC Consolidator Grants, jehož cílem je řešit zásadní vědecké otázky, v tomto roce usilovalo celkem 2 652 vědců působících ze 42 zemí. Z celkového počtu 313 úspěšných žadatelů jich nejvíce uspělo v Německu, Itálii, Francii, Velké Británii a Španělsku. V České republice získali v tomto roce ERC Consolidator pouze dva vědci. Vedle Aleny Zíkové to byl Pavel Plevka z výzkumného centra CEITEC Masarykovy univerzity. Více o jeho projektu si můžete přečíst zde.
Redakčně upraveno.
Zdroj: Biologické centrum AV ČR, Technologické centrum AV ČR
- Autor článku: ne
- Zdroj: Akademie věd ČR











































